ワクチン配分の政策と倫理
(こちらは、2008年に設置され5年間活動した生命・医療倫理政策研究ユニットによる、CBEL(The University of Tokyo Center for Biomedical Ethics and Law/東京大学グローバルCOE 次世代型生命・医療倫理の教育研究拠点創成)の研究成果を踏まえた政策レスポンスです)
2009年のH1N1インフルエンザの流行が提起する問題
多くの人が免疫を持たない感染症のワクチンの配分は、日本のみならず、世界的な問題である。「ワクチンの確保」「接種の優先対象」「ワクチンの入手と安全性」について、現在の主な議論を紹介する。なお、末尾にワクチンの配分に関するWHO専門委員会の勧告、米国CDCの専門委員会勧告(共に7月)の概要を紹介したので、併せて参照にされたい。(付表)
WHOによれば、ワクチン接種は最も安価な感染症対策の一つとされ、目標集団をあらかじめ設定できること、生活習慣の変化などを要さないなどの特徴を持った介入手段とされる。その一方、ワクチンの副作用の問題にはじまり、ワクチンの確保、アクセスの公平性など、多様な検討を要する側面もある。H1N1 インフルエンザ(‘H1N1 flu’以下、「新型インフル」)の感染者は日を追って増加し、7月に入って5千人を突破した。感染者の大半が軽症であるためか、メディアの報道は発生当初と比べて減っているようだ。しかし、もし不幸にも死者が出れば、再び発生当初のような混乱が生じうる懸念がある。また、ワクチンの作成にまだ成功していないこと、重症者に健常だった若者が多いことなど、通常の流行とは異なる対応が求められていることは間違いない。
1.ワクチン確保の国際競争と日本
- 「現在の世界のワクチン製造能力は、1年間で10億から20億回分のワクチンしかない」(米ウォールストリートジャーナル紙、5月16日)。季節性インフルエンザへの対応や一人当たり複数回の接種が必要であることなどを考慮すれば、新型インフルのワクチンを利用できる人びとは、たとえそれが早く完成しても、一部の人間に限られると指摘される。
- 日本国内では、予防接種への不信感の高まりを受けて、80年代にワクチンの製造量が落ち込んだ経緯がある。その後、徐々に製造量は回復したが、日本国内でワクチンの製造を手がける4つの機関は、いずれも規模が小さく生産能力には限界がある。厚生労働省は、7月中旬に季節性インフルエンザワクチンの生産を取りやめ、新型インフルのワクチン製造に切り替えることを表明した。当初は、2009年末までに約2500万人分のワクチンを調達することができるとみていたが、のちに下方修正した(2千万人を割る見込み)。一方、ワクチン投与対象を、ほぼ国民の半数にあたる約5千万人とし、不足分を輸入する方針を発表した(7月)。
- 日本では過去にも、海外から緊急的にワクチンを輸入したことがある(例えば、1961年の小児まひ[流行激化、国産ワクチンの不合格]、1970年の天然痘[後遺症問題])。この時も確保する量は問題になったが、それでも接種対象者は限られており、基本的には日本のニーズに応じた判断ができた。しかし、今回は、日本以外の多くの国もワクチンの入手を希望している。現在、こうしたワクチンの入手について、経済原理以外の制約は明確でない。多くの国が、「ワクチンの確保には問題がないが、時間がかかる」と留保を付している背景には、ワクチンが完成する日程が明確でなく、またそのワクチンの性格や使用条件が分からないということに加え、ワクチンの調達をめぐる「なりふり構わない奪い合いへと発展しかねない」(英国Guardian紙、7月17日)競争が国家間で起こっている背景がある。WHOのマーガレット・チャン事務局長は、先進国の買い占めにより貧困国が影響を受けることへの懸念を表明し、医療従事者へのワクチン接種はすべての国の医療基盤を守るために必要であること、各国が必要に応じて国内でのワクチンの配分を決定できるようにするべきことを強調している。
- この点について、ワクチンの製造拠点が集中するヨーロッパの動向は注視される。イギリスやフランス、スウェーデン、スイスなどは、ほぼ全人口分に匹敵する量のワクチンを確保する方針を表明している(その後、ギリシャやイスラエルも同様の方針を明らかにした)。特定の国家が、世界的に不足しているワクチンを大量に確保することは、これからワクチンを入手しようとする国にとってはアクセスの妨げに他ならず、国家間での助け合いに向けた取り組みに反するものとも評されている。一方、ドイツは、人口の3分の1にあたる人数分のワクチンを確保して医療者などに配分することで対応できるとする表明を示しているが、これはワクチン不足にも配慮した妥当な数値と評されている。
- また、ワクチンの研究開発と成果の還元を巡る議論もある。連帯の精神による国家間協力は、グローバル時代における感染症流行の抑制につながり、援助国にとっても長期的には恩恵となるという主張がその一つである(フランス国家生命倫理委員会、2009)。過去に、鳥インフルエンザのワクチン開発において、感染者が多く発生しワクチンのニーズが高い国が、ウイルス検体の提供という形でワクチンの研究開発に貢献を求められた上で、製品化されたワクチンの購入を迫られることは構造的な不公平であるとする抗議(インドネシア政府)が表明されたことがある。今回も製品開発されるワクチンの利益配分という、南北世界間での対立構造の本質は残ったままである。
- 政府には自国民を保護する使命があるが、一方で日本は世界の中でも高度の医療体制を備える国でもある。ワクチンをどのような必要性に基づいてどれほど確保するのか、その妥当性については広く国際的視点から考えるべきである。
2.誰を優先して接種対象にするべきか
- 予防接種法によると、予防接種は「伝染の恐れがある疾病の発生およびまん延の予防」の手段であるとされる(第一条)。他者への感染の防止が、接種を受けた本人への感染防止を通じて達成されることから、個人の健康・生命の保護と、他者及び一般社会の益との両方の側面がある。しかし、これらの両立は、接種のための完成されたワクチンが存在し、かつ資源が十分にあることが前提である。一方、資源が希少であるにもかかわらず、その資源を必要とする人が資源量以上に存在する場合、配分の順番を決める必要が生じる。「おなかをすかせた人たちがみなパイをほしがっているが、皆に行き渡る十分なパイがない場合にどのように分ければよいか」「救命ボートの数が限られている場合に誰を助けるべきか」などの古典的事例において公正な手順とは何かが問われてきた注)。ワクチンの配分についても、価値判断によって、例えば「子どもを優先するべき」(国の将来への恩恵という観点から)、「若年者層を優先するべき」(日常生活へのコストの観点から)、「健康で長く生きる者を優先」などの主張がある。一方、医療の恩恵が特定の個人に限定されるような状況は認めがたく、医学的リスクと直接関係しない基準で人を価値づけして優先順位を決定するべきではないとする反論もある(イギリス保健省インフルエンザ倫理委員会 2007年、フランス国家生命倫理委員会2009年)。
- パンデミックの発生は必ずしも新しい現象ではないが、交通量の増大とスピード化の時代の中で、以前にも増して全地球的な検討課題となっており、各国は感染症へのワクチン投与の優先順位に関するプランを検討してきた。その中で比較的共通して挙げられてきた優先対象は主に以下の①〜③の3群である。日本では、主に①、②について詳細なリスト案が公開されている(厚生労働省「新型インフルエンザワクチン接種に関するガイドライン」2007年、内閣府「新型インフルエンザワクチン接種の進め方について(第一次案)」2008年)。
| ① | 医療従事者 | 医療従事者一般をさす場合のほか、特に感染した患者との接点が多い者に限る場合などがある。 |
| ② | 社会基盤の維持に従事する者 | 秩序や非常時のインフラ管理を担う者(治安維持、消防、運輸など)。 |
| ③ | 感染による害が大きい者 | 新型インフルに関連して挙げられた区分としては、「妊婦」「高齢者(患者は少ないが、免疫を持たない者も多いとの所見による)」「若年者層(感染者が多い)」「児童(感染者が多い、集団行動が多い)」「乳児」「糖尿病」「肥満」。 |
- 但し、実際に伝播するウイルスの性質(どのような人が感染しやすいか、重症化しやすいかなど)により、対応の仕方は大きく異なる。日本を含め、各国の政府は、過去の議論を参考にしつつも、流行が起こるたびに実情に即して、優先すべき価値を最大化する方策を検討する必要がある。そのため、過去に立案したプランをそのまま利用するというわけにはいかない。
- 今回の新型インフルでは、感染者が死に至る割合が幸いにして少ないこともあり、各国の議論は上記のうち、特に「③感染による害が大きい者」に集中している。例えば、WHO(2009)やイギリスの保健省(2009)による方針では、いずれも「疫学的根拠」の把握が重要視されている。流行の状況は先進国間でも大きく異なることから、日本の流行の実態に即して順番を考える必要があるだろう。
- なお、この種の方針決定には社会的な懸念が大きいことから、流行前からの情報提供や社会の関心の向上を高めるためのインフラを整備する必要がある。たとえば、アメリカが各州・自治体に示した計画立案の指針では、流行前からの「パブリックヘルス・コミュニケーション」を通じた情報共有の重要性を指摘している(アメリカ厚生省、2005)。また、行政当局において、感染症対策における倫理問題を検討し、政策立案に関する提言を行う委員会が活動している例もある(例:アメリカCDC「公衆衛生倫理委員会」ほか、イギリス保健省「パンデミック・インフルエンザ倫理委員会」)。
3.ワクチンの試験と安全性
- ワクチンは、病原体(ウイルス)の性質を利用した医薬品で、抗体を作るために体内に注入されるものである。日本ではワクチンそのものによる副作用等による被害が大きな社会的懸念をもたらし、その後のワクチン行政の萎縮的な運用を招いたと指摘される。
- 現在、新型インフルに対応するワクチンはまだ完成していない。アメリカ、オーストラリア、中国によるワクチンの臨床試験計画が発表されたばかりである。現状では、注入するワクチンの量、接種後の身体への影響等、ワクチンの基本的な性格を把握するための試験に数週間から数か月を要するとされている。さらに製品化後も、実際にたくさんの人々に使用された状況で発生する問題を把握するために、市販化後調査が必要となる。
- こうした中、通常の季節性インフルエンザが流行する時期が迫る前に、ワクチンを完成させ、かつ普及させたいという国が登場し、議論を複雑にしている。特にヨーロッパでは、感染者が集中するイギリスなどによって、安全性や有効性に関するデータ提出を簡略化した迅速審査が求められ、ヨーロッパ医薬品庁(EMA)がこれに応じて審査手順の簡略化の方針を示している。一方、WHOはこうした手法ではワクチンの質が確保できない可能性があるとして批判している。また、アメリカでは、1976年にH1N1型の豚インフルエンザが流行した際、発生した合併症によりワクチン接種事業が中断された経緯から、審査手順の簡略化に反対する世論が根強くある。日本がワクチンを輸入するとなれば、入手できる時期のみではなく、どのような試験を経たワクチンであるのか、臨床試験の質を踏まえた判断が求められるだろう。
付表 新型インフルエンザ(H1N1)に関するワクチンの配分方針(2009年7月末現在)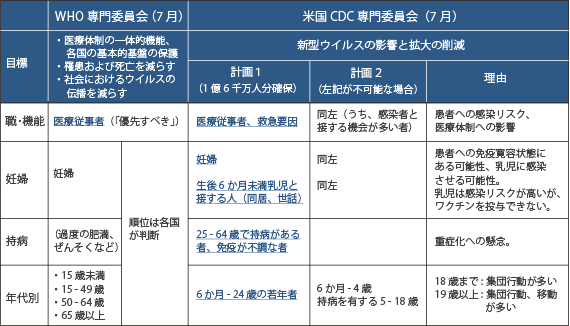
出典:World Health Organization, Global Alert and Response (WHO recommendations on pandemic (H1N1) 2009 vaccines), 2009(July), US Centers for Disease Control and Prevention, CDC Advisors Make Recommendations for Use of Vaccine Against Novel H1N1, 2009(July).



